
Af Peter F. Gammelby 19.11.2016
Det svarer til at udvikle et våben, der er lige så kraftigt som de hidtil kendte, men seks gange så præcist. Fordelene er indlysende: man behøver ikke at bruge så mange af dem for at få has på fjenden, og risikoen for at skade civile i nærheden er tilsvarende mindre.
Fjenden er i denne sammenhæng kræftceller inde i ondartede svulster, mens civilisterne er raske celler i nærheden.
Og det nye præcisionsvåben er cellegiften BE-43547A, som normalt kun produceres af bakterier i jorden og havbunden, hvor ilten er sparsom.
Dér bruger bakterierne med stor sandsynlighed giften mod konkurrerende mikroorganismer, men da giften har den egenskab at kunne angribe såkaldt hypoxiske celler – celler som stort set ikke behøver ilt – er den også effektiv mod hypoxiske kræftceller, der opstår under udvikling af kræftsvulster og medvirker til metastase.
Nu er det lykkedes et tværfagligt forskerhold på Aarhus Universitet at syntetisere en nøjagtig kopi af cellegiften, og tillige opdage nye bakterier, som også kan fremstille stoffet. Deres resultater er netop offentliggjort i det prestigefyldte videnskabelige tidsskrift Nature Chemistry.
En del af forskerne har allerede en vis rutine i at syntetisere naturstoffer til potentiel brug i sygdomsbehandling. I 2015 lykkedes det dem at syntetisere en anden cellegift fra bakterier, rakicidin A, som også dræber hypoxiske celler.
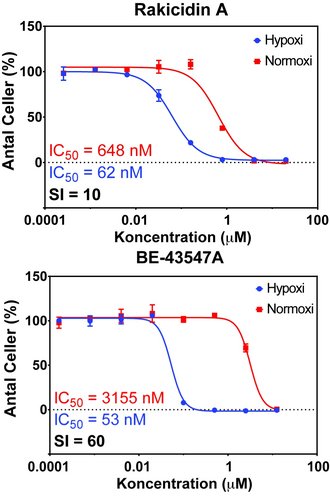
Det nye stof, BE-43547A er et ”søsterstof” til rakicidin A, men selv om de to stoffers molekylære strukturer ligner hinanden, har forskerne nu påvist, at BE-43547A er op til seks gange mere præcist – eller selektivt – når det gælder om at angribe hypoxiske celler, end rakicidin er.
Det skal forstås sådan, at begge cellegifte slår hypoxiske celler ihjel og lader normoxiske celler i fred, hvis man giver dem i begrænsede doser; i højere doser er de skadelige for alle celler. Men man kan altså nøjes med lavere doser af BE-43547A end af rakicidin A for at opnå den samme effekt – og man kan om nødvendigt give højere doser BE-43547A end af rakicidin, uden at skade de normale celler.
”Vores nye stof er meget mere interessant end rakicidin, fordi det går endnu mere præcist efter hypoxiske celler. Ifølge vore undersøgelser findes der ikke et andet naturstof med så høj selektivitet som BE-43547A. Og da det er lettere end rakicidin at syntetisere, kan det i princippet opskaleres til prækliniske forsøg. Vi fokuserer dog i øjeblikket på at forsimple den molekylære struktur af disse stoffer, som vi samlet kalder for APD-CLD’er – et akronym der beskriver stoffernes særlige kemiske sammensætning”, forklarer adjunkt Thomas Bjørnskov Poulsen, hvis laboratorium på Institut for Kemi på Aarhus Universitet har specialiseret sig i at finde og kopiere naturstoffer, der virker mod kræft.
Til undersøgelserne af BE-43547A har han yderligere allieret sig med kollegaer fra Institut for Kemi og Institut for Retsmedicin på Aarhus Universitet samt hos Interdisciplinary Nanoscience Center (iNANO), særligt adjunkt Thomas Tørring, som arbejder med at klarlægge mikroorganismers evne til at fremstille komplekse naturstoffer, og som også er seniorforfatter på artiklen i Nature.
Thomas B. Poulsen modtog i foråret en Sapere Aude-bevilling på godt syv mio. kr. fra Det Frie Forskningsråd til at forfine et molekyle fra APD-CLD-familien og afprøve det på pankreas-kræftceller (kræft i bugspytkirtlen) i prækliniske forsøg – altså laboratorieforsøg på mus.
Videnskaben har anset BE-43547A som et potentielt middel mod visse kræftsvulster, siden et hold japanske forskere isolerede cellegiften i 1998. Ved samme lejlighed tog et japansk firma patent på at udvinde stoffet fra en specifik bakteriestamme og bruge det mod kræftsvulster. Siden har der ikke været publiceret forsøg med den.
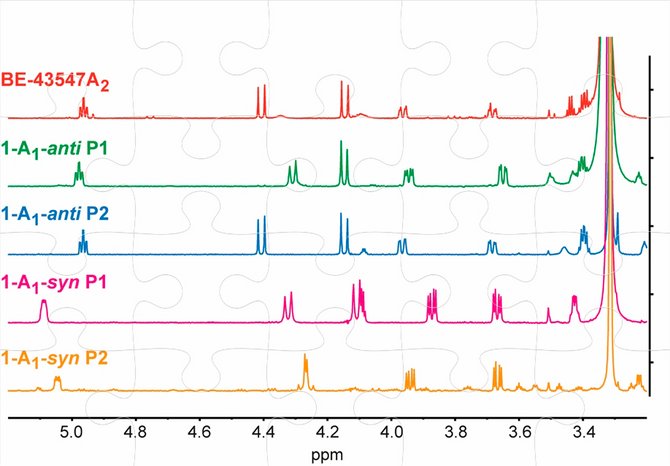
Thomas B. Poulsens laboratorium satte sig i 2012 for at konstruere både rakicidin A og BE-43547A for at kunne sammenligne stoffernes biologiske aktiviteter. Ud fra BE-43547A’s kemiske bestanddele syntetiserede de fire forskellige molekyler – en for hver af dens mulige rumlige strukturer.
Men til forskernes store overraskelse viste NMR-spektroskopiske undersøgelser, at ingen af deres syntetiserede molekyler matchede de signaler, som var rapporteret for det naturlige molekyle, japanerne havde patenteret.
”Vi mente, at japanernes beskrivelse af molekylets struktur måtte være forkert. Men da vi ville analysere stoffet fra naturens mikroorganismer forfra, fandt vi ud af, at den oprindelige mikroorganisme, som det japanske firma lavede patent ud fra, er ”trukket tilbage” fra den biobank i Korea, der opbevarede den. Så vi måtte i gang med at lede efter nogle andre mikroorganismer, som laver den samme cellegift,” forklarer Thomas B. Poulsen.
Eftersøgningen efter egnede kandidater foregik dog uden brug af dykkerdragt, skovl og lup.
I stedet fandt forskerne nogle specifikke gen-sekvenser i den bakterie, som producerer rakicidin, og søgte efter lignende sekvenser i databaser over genomer fra mikroorganismer over hele verden ved hjælp af værktøjet BLAST (Basic Local Alignment Search Tool).
BLAST’s algoritmer er så hurtige og effektive, at det at blaste en sekvens er blevet et fagudtryk. Værktøjet bruges ofte til at afsløre funktionen af forskellige DNA- og proteinsekvenser, idet man går ud fra, at to sekvenser, hvis aminosyresammensætning ligner hinanden tilstrækkelig meget, også har den samme funktion.
”Vi gik ud fra, at hvis der er andre mikroorganismer, som har disse gen-sekvenser, er der en sandsynlighed for, at de også kan producere hypoxia-selektive gifte. Ud fra BLAST-hittene identificerede vi to forskellige mikroorganismer hos forskningslaboratorier i Tyskland og USA, som viste sig at kunne producere BE-43547A. Det var der ingen, der vidste, at de kunne,” fortæller Thomas Tørring fra iNANO.
NMR-spektroskopi af de ”nye” bakteriers naturlige cellegift matcher et af forskernes syntetiserede BE-43547A-molekyler.
Spektroskopien er ganske vist ikke i sig selv en garanti for, at forskerne har ramt plet. Det er nemlig næsten umuligt at få et præcist billede af det pågældende molekyles rumlige struktur, fordi det vrider og vender sig, så man får et billede af en ”gennemsnitsstruktur” af molekylet over tid.
”Sådan er det nu, og det var bestemt ikke lettere for japanerne i 1998. Når vi alligevel nu kan være meget sikre på at have tilordnet den korrekte struktur, er det en kombination af, at vi har fremstillet molekylet i alle dets teoretisk mulige former, samt har unik indsigt i, hvordan molekylet fremstilles i mikroorganismerne,” siger Thomas B. Poulsen.